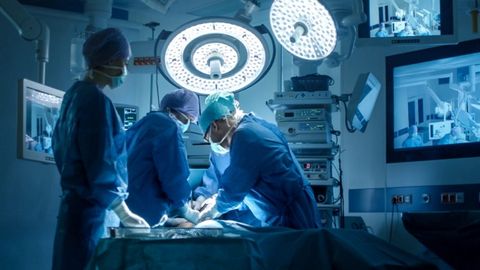
Investigadores canadienses han desarrollado enzimas que convirtieron con éxito el órgano de un paciente en muerte cerebral al tipo 0, válido para cualquier trasplante, un avance que podría acelerar la compatibilidad de las donaciones
17 oct 2025 . Actualizado a las 13:40 h.Un equipo internacional de científicos ha dado un paso que podría ser crucial en el campo de los trasplantes de órganos al realizar con éxito el primer trasplante humano de un riñón modificado del tipo sanguíneo A al tipo universal O. Este logro, publicado en la revista Nature Biomedical Engineering, se basa en el uso de enzimas especiales desarrolladas en la Universidad de Columbia Británica (UBC) que «cortan» los azúcares que definen el grupo sanguíneo, convirtiendo el órgano en tipo O, apto para cualquier receptor.
Este avance es particularmente importante para los pacientes con sangre tipo O, que representan más de la mitad de las listas de espera de riñón y que a menudo esperan de dos a cuatro años más, debido a que solo pueden recibir órganos de su mismo tipo.
Para demostrar la viabilidad del método sin poner en riesgo una vida, el riñón transformado enzimáticamente fue trasplantado a un receptor con muerte cerebral con el consentimiento de su familia.

Durante dos días, el riñón funcionó sin signos de rechazo híperagudo, la rápida reacción inmunitaria que puede destruir un órgano incompatible en cuestión de minutos. Al tercer día, reaparecieron algunos marcadores del tipo sanguíneo, lo que provocó una reacción leve, pero el daño fue mucho menos grave que en una incompatibilidad típica, y los investigadores observaron indicios de que el organismo comenzaba a tolerar el órgano.
«Esta es la primera vez que observamos este proceso en un modelo humano», afirmó el doctor Stephen Withers, profesor emérito de química de la UBC, quien codirigió el desarrollo de la enzima. «Nos proporciona información invaluable para mejorar los resultados a largo plazo», añadió.
Este avance es el resultado de más de una década de trabajo. A principios de la década del 2010, el doctor Withers y su colega Jayachandran Kizhakkedathu, profesor de la UBC en el departamento de Patología y Medicina de Laboratorio y en el Centro de Investigación de la Sangre, se centraron en generar sangre universal para donantes eliminando los azúcares que definen los grupos sanguíneos.
Esos mismos azúcares, o antígenos, recubren los vasos sanguíneos de los órganos. Si el sistema inmunitario del receptor detecta el antígeno equivocado, lo ataca. Los pacientes con tipo O (más de la mitad de las listas de espera de riñón) solo pueden recibir órganos de este tipo. Sin embargo, estos riñones suelen donarse a otros debido a su compatibilidad universal. Como resultado, los pacientes con tipo O suelen esperar de dos a cuatro años más, y muchos mueren durante la espera.

Los métodos tradicionales para superar la incompatibilidad de tipo sanguíneo en trasplantes requieren días de tratamiento intensivo para eliminar los anticuerpos y suprimir el sistema inmunitario del receptor, además de requerir órganos de donantes vivos. Este nuevo enfoque cambia el órgano en lugar del paciente, lo que significa que los trasplantes podrían realizarse más rápido, con menos complicaciones y, por primera vez, podría permitir el uso de órganos de donantes fallecidos con incompatibilidad de tipo sanguíneo, momento en el que cada hora puede determinar la vida o la muerte de un paciente.
La clave de este enfoque fue el descubrimiento, en el 2019, por parte del equipo de la UBC de dos enzimas altamente eficientes que eliminan el azúcar (antígenos) que define la sangre tipo A, convirtiéndola eficazmente en tipo O. «Estas enzimas son muy activas, altamente selectivas y funcionan en concentraciones muy bajas», explica Kizhakkedathu. «Eso hizo viable todo el concepto».
El siguiente reto fue aplicar esto a órganos completos, lo que se logró en el 2022 cuando un equipo de Toronto demostró que los pulmones podían transformarse. Tras realizar pruebas exitosas con sangre, luego pulmones y riñones (con la Universidad de Cambridge) fuera del cuerpo, la pregunta persistía: ¿Podría un órgano transformado enzimáticamente sobrevivir dentro del sistema inmunitario humano?
La respuesta llegó a finales del 2023 durante un viaje al extranjero del doctor Kizhakkedathu. «Nuestros colaboradores me mostraron sus datos: usando nuestras enzimas, habían transformado un riñón humano y lo habían trasplantado a un receptor con muerte cerebral. Estaba funcionando de maravilla». Se quedó despierto hasta tarde para llamar al Dr. Withers a primera hora de la mañana en el Centro de Salud. «Estaba tan emocionado. Fue un momento de ensueño».
Los antígenos del tipo sanguíneo actúan como etiquetas en las células, y las enzimas identificadas por la Universidad de Columbia Británica actúan como tijeras moleculares, cortando la etiqueta que identifica al tipo A y revelando el tipo O que se encuentra debajo. «Es como quitar la pintura roja de un coche y descubrir la imprimación neutra», apunta de forma gráfica el doctor Withers. «Una vez hecho esto, el sistema inmunitario ya no percibe el órgano como extraño».
La aprobación regulatoria para ensayos clínicos será la próxima prueba de fuego, aunque todavía quedan desafíos por resolver. Avivo Biomedical, una empresa derivada de la universidad canadiense, liderará el desarrollo de estas enzimas para su aplicación en trasplantes y para permitir la creación de sangre de donantes universales a demanda para la medicina transfusional. El potencial es enorme. «Así es como se ve cuando años de ciencia básica finalmente se conectan con la atención al paciente», dijo el doctor Withers. «Ver cómo nuestros descubrimientos se acercan cada vez más al impacto en el mundo real es lo que nos impulsa a seguir adelante».
